GMP nel settore farmaceutico: Come individuare i difetti – Seconda parte
Nella prima parte del nostro viaggio tra i potenziali difetti che possono verificarsi nella produzione e confezionamento di farmaci, ci siamo soffermati sui dati critici stampati sulla confezione e sui difetti del farmaco stesso. Oggi parliamo delle altre due macroaree di potenziali difetti: quelli riguardanti la confezione e quelli sui dati variabili.
Difetti riguardanti la confezione
Per confezione si intende l’insieme di involucri protettivi che hanno lo scopo di proteggere il farmaco e salvaguardare il suo trasporto.
Confezione incompleta
Per confezione incompleta si intende una confezione totalmente o parzialmente priva di una delle sue parti. Pensiamo, ad esempio, a una confezione che dovrebbe contenere dieci bustine di farmaco e invece ne conta solo otto. In questo caso possiamo parlare di confezione incompleta e il paziente potrebbe trovarsi nella condizione di non poter completare il ciclo di cura prescritto.
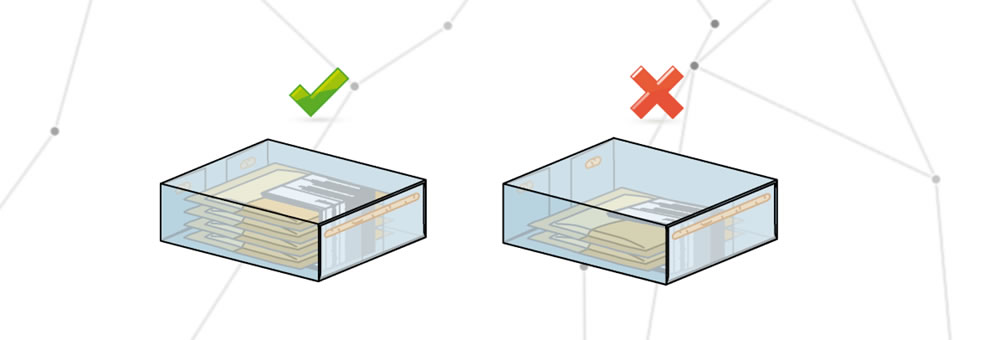
Confezione non corretta
Una confezione non corretta contiene uno o più elementi che non sono previsti dal rapporto di confezionamento.
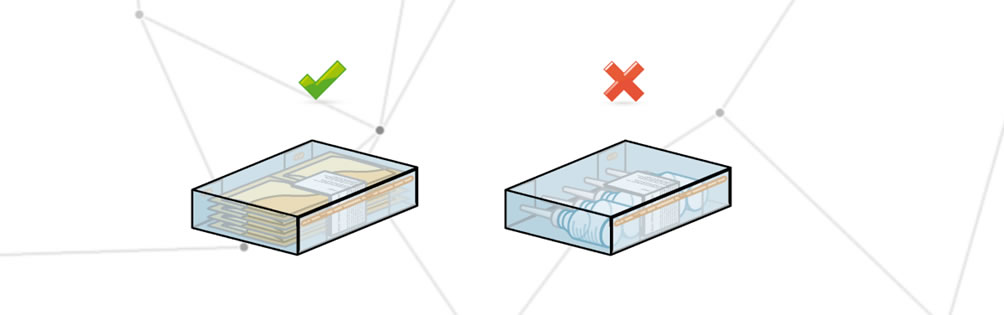
Confezione sporca
La confezione viene definita sporca quando presenta parti estranee che possono cambiare l’aspetto o rendere illeggibili le informazioni presenti sulla confezione.
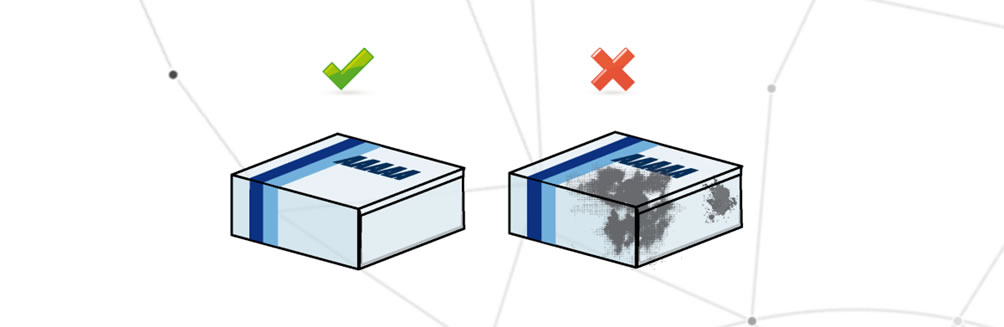
Confezione danneggiata
La confezione viene danneggiata quando uno o più elementi di confezionamento presenta danni estetici.
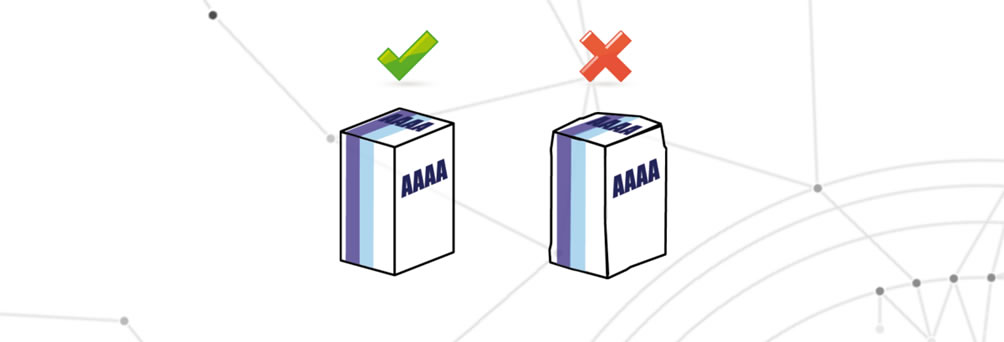
Difetti riguardanti i dati variabili
I dati variabili sono stampati sulla confezione durante il confezionamento del farmaco o memorizzati sui sistemi da convalidare. Si tratta di informazioni importanti quali, ad esempio, la data di scadenza, il numero del lotto e altri parametri.
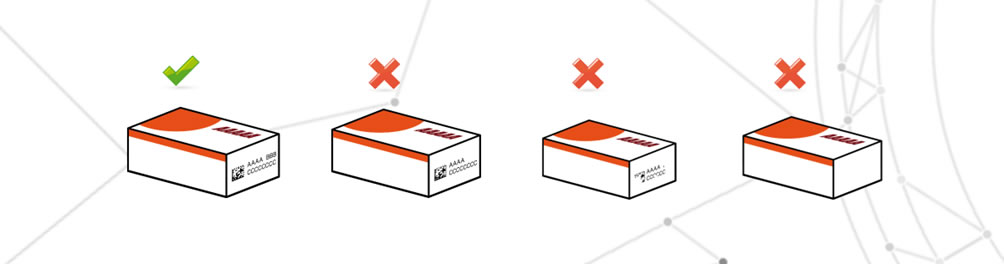
Illeggibilità dei dati variabili
Per illeggibilità dei dati variabili si intende: completa mancanza, presenza parziale, stampa non nitida.
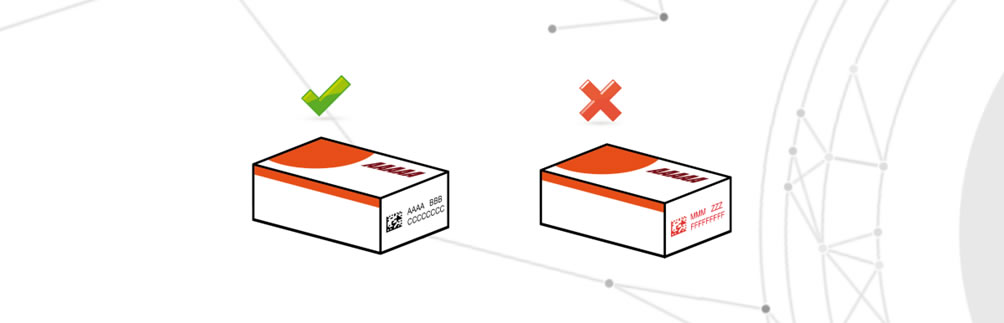
Dati variabili errati
Per dati variabili errati si intende la stampa di informazioni errate rispetto a quelle previste dal rapporto di confezionamento.
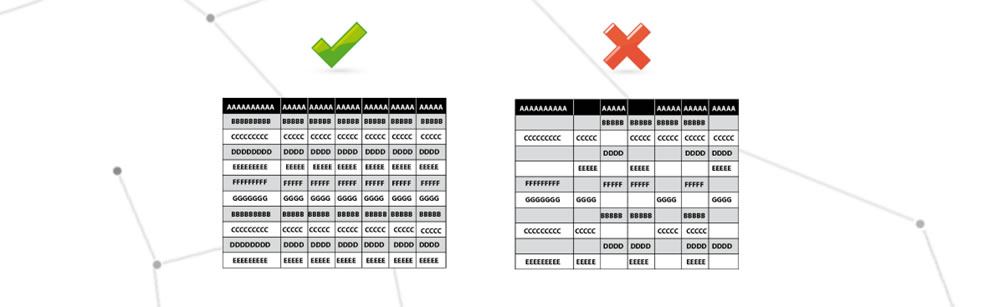
Perdita di informazioni critiche per le GMP
Per informazioni critiche GMP si intendono le informazioni memorizzate sui sistemi da convalidare che contengono parametri critici, ad esempio per serializzare il farmaco, la registrazione di parametri critici, le modifiche apportate al processo.
GMP nel settore farmaceutico: Come individuare i difetti – Prima parte
Foto di Karolina Grabowska da Pexels




